Osmosis didefinisikan sebagai aliran bersih atau pergerakan molekul pelarut melalui membran semipermeabel yang tidak dapat dilewati oleh molekul terlarut. Jika larutan penyangga terdiri dari molekul terlarut dan pelarut ditempatkan di satu sisi membran dan pelarut murni ditempatkan di sisi lain, ada aliran bersih pelarut ke sisi larutan membran. Tekanan osmotik merupakan faktor penting yang mempengaruhi sel.
Selain berkaitan dengan tubuh makhluk hidup, prinsip kerja tekanan osmosis juga bisa digunakan sebagai dasar penyaringan (“reverse osmosis“), suatu proses yang biasa digunakan dalam pemurnian air. Arti air yang akan dimurnikan ditempatkan dalam suatu bilik dan ditempatkan di bawah sejumlah tekanan lebih besar dari tekanan osmotik yang diberikan oleh air dan zat terlarut di dalamnya.
Tekanan Osmotik
Osmosis adalah difusi air tertentu melalui membran semi-permeabel. Jadi dalam kasus osmosis, zat terlarut tidak dapat bergerak karena mereka tidak dapat melewati membran. Namun, air dapat bergerak, dan melewati membran ke daerah dengan konsentrasi zat terlarut yang lebih tinggi.
Hal ini tentusaja dapat menyebabkan volume total air di setiap sisi membran berubah: sisi membran dengan lebih banyak zat terlarut mungkin berakhir dengan lebih banyak air. Hal ini dapat menyebabkan masalah bagi sel, seperti meledak (jika terlalu banyak air bergerak ke dalam sel), atau menjadi dehidrasi (jika terlalu banyak air bergerak keluar).
Ini adalah faktor yang sangat penting dalam biologi karena lingkungan intraseluler berbeda dari lingkungan ekstraseluler. Jika lingkungan ekstraseluler berubah, itu dapat menyebabkan air mengalir ke sel kita.
Beberapa organisme, seperti tanaman yang menggunakan tekanan osmotik untuk memindahkan air, telah mengambil keuntungan dari prinsip ini. Tapi itu juga dapat mengancam kesehatan sel dan organisme ketika ada terlalu banyak atau terlalu sedikit air di lingkungan ekstraseluler dibandingkan dengan bagian dalam sel.
Pengertian Tekanan Osmotik
Tekanan osmotik adalah tekanan minimum yang perlu diterapkan pada larutan untuk mencegah aliran masuknya pelarut murni melintasi membran semipermeabel. Ini juga didefinisikan sebagai ukuran kecenderungan solusi untuk mengambil dalam pelarut murni oleh osmosis.
Tekanan potensial osmotik adalah tekanan osmotik maksimum yang dapat berkembang dalam larutan jika dipisahkan dari pelarut murni oleh membran semipermeabel. Osmosis terjadi ketika dua larutan, yang mengandung konsentrasi zat terlarut yang berbeda, dipisahkan oleh membran selektif permeabel.
Molekul pelarut melewati secara istimewa melalui membran dari larutan konsentrasi rendah ke larutan dengan konsentrasi zat terlarut lebih tinggi. Transfer molekul pelarut akan berlanjut sampai kesetimbangan tercapai.
Pengertian Tekanan Osmotik Menurut Para Ahli
Adapun definisi tekanan osmotik menurut para ahli, antara lain:
- Biology Dictionary
Tekanan osmotik dapat dianggap sebagai tekanan yang diperlukan untuk menghentikan air agar tidak berdifusi melalui penghalang oleh osmosis. Dengan kata lain, ini mengacu pada seberapa keras air akan “mendorong” untuk melewati penghalang agar berdifusi ke sisi lain.
Tekanan osmotik ditentukan oleh konsentrasi zat terlarut - air akan “berusaha lebih keras” untuk berdifusi ke area dengan konsentrasi zat terlarut yang tinggi, seperti garam, daripada ke area dengan konsentrasi rendah.
Dalam kenyataannya tentu saja, tekanan osmotik bukanlah “keinginan” air untuk bergerak, tetapi lebih merupakan perpanjangan dari hukum alam bahwa semua materi akan terdistribusi secara acak dari waktu ke waktu.
Ketika konsentrasi zat berbeda di dua area dan area memiliki kontak satu sama lain, gerakan acak partikel akan menyebabkan zat tersebut berdifusi hingga larutannya seragam di seluruh area.
- Lumen Learning
Tekanan osmotik adalah tekanan yang perlu diterapkan untuk mencegah aliran air ke dalam membran semipermeabel. Tekanan osmotik juga dapat dijelaskan sebagai tekanan yang diperlukan untuk menghentikan osmosis.
Salah satu cara untuk menghentikan osmosis adalah dengan meningkatkan tekanan hidrostatik pada sisi larutan membran; ini pada akhirnya meremas molekul pelarut lebih dekat bersama, meningkatkan “kecenderungan melarikan diri.”
Kecenderungan pelarian dari larutan dapat dinaikkan sampai akhirnya sama dengan molekul dalam pelarut murni; pada titik ini, osmosis akan berhenti. Tekanan osmotik adalah tekanan yang diperlukan untuk mencapai keseimbangan osmotik.
Manfaat Tekanan Osmotik
Tekanan osmotik memiliki manfaat yang beragam, diantaranya yaitu:
-
Tekanan osmotik secara fisiologis
Tekanan osmotik berperan penting bagi proses fisiologis pada manusia, diantaraya yaitu:
- Penyerapan dari saluran pencernaan, juga pertukaran cairan di berbagai kompartemen tubuh mengikuti prinsip osmosis.
- Tekanan osmotik protein plasma mengatur air mengalir dari cairan usus bebas protein ke dalam pembuluh darah.
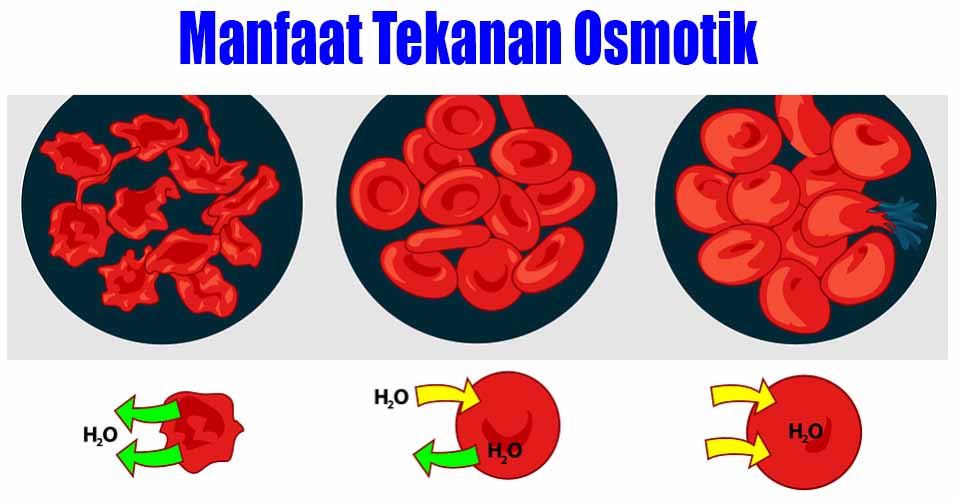
- Sel darah merah yang hidup, jika tersuspensi dalam larutan NaCl 0,92%, tidak mendapat atau kehilangan air. Secara singkat, cairan intraseluler sel darah merah adalah isotonik dengan membran sel darah merah dalam larutan NaCl 0,92%.
-
Penentuan berat molekul
Karena semua sifat koligatif larutan tergantung pada konsentrasi pelarut, pengukurannya dapat berfungsi sebagai alat eksperimental yang mudah untuk menentukan konsentrasi, dan dengan demikian berat molekul zat terlarut.
Tekanan osmotik sangat berguna dalam hal ini, karena sejumlah kecil zat terlarut akan menghasilkan perubahan yang jauh lebih besar dalam jumlah ini daripada pada titik didih, titik beku, atau tekanan uap. bahkan larutan 10-6 molar akan memiliki tekanan osmotik yang dapat diukur.
Penentuan berat molekul sangat sering dilakukan pada protein atau polimer dengan berat molekul tinggi lainnya. Zat-zat ini, karena ukuran molekulnya yang besar, cenderung hanya sedikit larut dalam sebagian besar pelarut, sehingga pengukuran tekanan osmotik seringkali merupakan satu-satunya cara praktis untuk menentukan bobot molekulnya.
-
Osmosis air laut dapat menghasilkan tenaga listrik
Prinsip kerja tekanan osmosis ternyata juga bisa dimanfaatkan untuk menghasilkan tenaga energi listrik yang bersumber dari air laut. Proses ini diawali dengan mengumpankan air tawar dan air laut ke pembangkit. Air laut dan air tawar akan disaring terlebih dahulu untuk menghilangkan pengotor.
Selanjutnya, air tawar dan air laut mengalami perbedaan perlakuan, air tawar akan langsung dimasukkan pada modul membran, sedangkan air laut akan diberikan tekanan tambahan sebelum masuk modul membran. Di dalam modul membran akan terjadi peristiwa osmosis yang menyebabkan 80-90% air tawar akan berpindah melalui membran ke air laut bertekanan.
Setelah keluar dari modul membran laju alir volumetric air bertekanan tinggi akan meningkat akan mengalir menuju turbin. Tetapi aliran air laut ini tidak semuanya menuju turbin melainkan sekitar 2/3 bagian akan diumpankan ke penukar tekanan untuk memberikan tekanan ke umpan air laut yang baru. Sisa air yang tidak diumpankan ke penukar tekanan akan mengalir melewati turbin dan menggerakkan turbin sehingga menghasilkan listrik.
-
Transportasi air pada tanaman
Aliran osmotik memainkan peran penting dalam pengangkutan air dari sumbernya di tanah ke pelepasannya oleh transpirasi dari daun, dibantu oleh kekuatan ikatan hidrogen antara molekul air.
Air masuk ke akar melalui osmosis, didorong oleh konsentrasi air yang rendah di dalam akar yang dikelola oleh transportasi aktif [non-osmotik] nutrisi ionik dari tanah dan oleh pasokan gula yang difotosintesis dalam daun.
Ini menghasilkan sejumlah tekanan akar tertentu yang mengirimkan molekul air dalam perjalanan mereka melalui saluran pembuluh darah batang atau batang. Tetapi tekanan akar maksimum yang telah diukur dapat mendorong air hanya sekitar 20 meter, sedangkan pohon-pohon tertinggi melebihi 100 meter.
Tekanan akar dapat menjadi satu-satunya penggerak transportasi air pada tanaman pendek, atau bahkan pada tanaman tinggi seperti pohon yang tidak ada daunnya. Tetapi ketika tanaman yang lebih tinggi secara aktif melakukan transpirasi (kehilangan air ke atmosfer), osmosis mendapat dorongan dari apa yang disebut oleh fisiologis tumbuhan sebagai ketegangan kohesi atau tarikan transpirasional.
Karena setiap molekul H2O muncul dari lubang di daun, ia menarik sepanjang rantai molekul di bawahnya. Jadi ikatan hidrogen tidak kalah pentingnya dengan osmosis dalam keseluruhan proses transportasi air.
-
Proses Cuci Darah (Dialisis)
Prinsip tekanan osmotik dapat diaplikasikan dalam bidang medis yaitu pada proses cuci darah atau yang juga dikenal dengan dialisis. Dalam bidang medis, cuci darah sangat penting bagi pasien penderita gagal ginjal yang diakibatkan oleh disfungsi ginjal sehingga tidak bisa berfungsi dengan semestinya untuk melakukan filtrasi darah.
Teknologi dialisis memungkinkan proses filtrasi darah dilakukan di luar ginjal menggunakan suatu mesin. Cara kerja dari mesin ini yaitu darah dari tubuh akan dimasukkan ke dalam mesin dan akan melalui suatu membran semipermeabel.
Melalui membran tersebut, kotoran dalam darah bisa dipisahkan melalui membran dialisis untuk terpisah dari darah sehingga akan didapatkan darah hasil cuci yang bebas dari pengotor.
-
Untuk pengawetan makanan
Prinsip kerja tekanan osmotik dapat digunakan dalam industri makanan yaitu untuk proses pengawetan makanan. Hal tersebut dapat dilakukan dengan memanfaatkan terjadinya krenasi pada sel dimana untuk mengawetkan makanan, industri makanan biasanya menggunakan gula dengan jumlah banyak untuk menghasilkan larutan konsentrasi tinggi.
Dengan larutan yang berkonsentrasi tinggi atau hipertonik, maka saat ada bakteri yang datang tidak bisa bertahan hidup lama sebab air dalam sel bakteri akan mengalami osmosis keluar dinding sel menuju larutan gula dengan konsentrasi tinggi.
Akibatnya adalah sel pada bakteri mengalami peristiwa krenasi yang mengakibatkan sel mengerut sehingga kehilangan fungsinya dan membuat bakteri tersebut mati. Dua zat yang paling umum digunakan untuk menciptakan lingkungan hipertonik bagi mikroorganisme dan mencegahnya tumbuh adalah garam dan gula.
- Garam untuk pengawetan daging
Garam meja (natrium klorida) adalah bahan utama yang digunakan dalam pengasapan daging. Penghapusan air dan penambahan garam ke daging menciptakan lingkungan yang kaya zat terlarut di mana tekanan osmotik menarik air dari mikroorganisme, sehingga memperlambat pertumbuhannya. Melakukan ini memerlukan konsentrasi garam hampir 20%.
- Gula untuk pengawetan buah-buahan
Gula digunakan untuk mengawetkan buah-buahan, baik dalam sirup dengan buah-buahan seperti apel, pir, persik, aprikot, prem atau dalam bentuk kristal di mana bahan yang diawetkan dimasak dalam gula sampai titik kristalisasi dan produk yang dihasilkan kemudian disimpan kering.
Tujuan dari gula adalah untuk menciptakan lingkungan yang tidak bersahabat dengan kehidupan mikroba dan mencegah pembusukan makanan. Dari waktu ke waktu, gula juga telah digunakan untuk pengawetan non-makanan.
Misalnya, madu digunakan sebagai bagian dari proses mumifikasi di beberapa ritus Mesir kuno. Namun, pertumbuhan jamur dan jamur tidak ditekan seefisien pertumbuhan bakteri.
-
Pemurnian atau Desalinasi Air Laut
Agar air laut bisa digunakan dan dikonsumsi, maka perlu adanya pemurnian air dari zat terlarut yang ada pada air laut. Hal ini bisa dilakukan dengan menerapkan prinsip kerja tekanan osmotik, yaitu dengan memberikan tekanan yang lebih besar dari tekanan osmotik air laut tersebut sehingga air sebagai pelarut akan melalui membran semipermeabel, meninggalkan zat terlarut pada air laut yang tidak dapat melalui membran.
Proses tersebut disebut sebagai osmosis balik dimana pelarut dalam kondisi konsentrasi tinggi akan melalui membran semipermeabel menuju konsentrasi rendah. Tapi apabila proses ini dilakukan tanpa menggunakan tekanan yang besar maka yang akan terjadi sebaliknya, yaitu air murni justru akan masuk ke dalam air laut.
-
Pemurnian air limbah
Bukan hanya untuk memurnikan air laut, prinsip kerja tekanan osmotik juga bisa digunakan sebagai pemurnian air limbah cair untuk menghilangkan zat zat berbahaya sebelum dibuang ke lingkungan, yaitu melalui pengaplikasian reverse osmosis (RO) atau osmosis balik. Sama halnya ketika akan memurnikan air laut.
Reverse Osmosis menerapkan tekanan yang lebih besar dari tekanan osmotik (antara 2-10 Mpa) ke dalam larutan konsentrat, sehingga mengakibatkan larutan mengalir dari sisi konsentrat membran semipermeabel ke dilute side.
RO mempunyai kemampuan menyingkirkan total dissolved inorganic solid 95-99,5% dan dissolved organic solid 95-97%. Teknologi tersebut sudah digunakan untuk menyingkirkan radionuklida dari limbah cair level rendah seperti limbah uap dari pembangkit tenaga nuklir.
-
Prinsip kerja infus
Prinsip kerja infus pada dasarnya menerapkan tekanan osmotik. Prinsip tekanan osmotik dalam penggunaan infus adalah contoh penerapan sifat larutan koligatif di bidang kesehatan. Penemu prinsip tekanan osmotik sebagai salah satu sifat koligatif larutan adalah Jacobus Henricus van’t Hoff.
Ia adalah pemenang nobel kimia tahun 1901 atas penelitiannya pada kimia kinetik tentang makna kesetimbangan kimia, tekanan osmotik, dan kristalografi. Penelitiannya yang berkaiatan dengan tekanan osmotik menunjukkan bahwa tekanan osmotik suatu larutan sebanding dengan konsentrasi dan suhu larutan tersebut.
-
Prinsip kerja minuman pengganti ion tubuh
Prinsip tekanan osmotik bukan hanya digunakan pada cairan infus, tapi minuman-minuman pengganti ion tubuh yang kini marak di kalangan masyarakat juga menggunakan prinsip ini sebagai dasar pembuatannya.
Nah, itulah tadi penjelasan serta pengulasan secara lengkap kepada segenap pembaca terkait dengan manfaat tekanan osmotik secara umum bagi kehidupan manusia. Semoga melalui materi ini bisa memberikan wawasan dan menambah pengetahuan bagi pembaca sekalian.