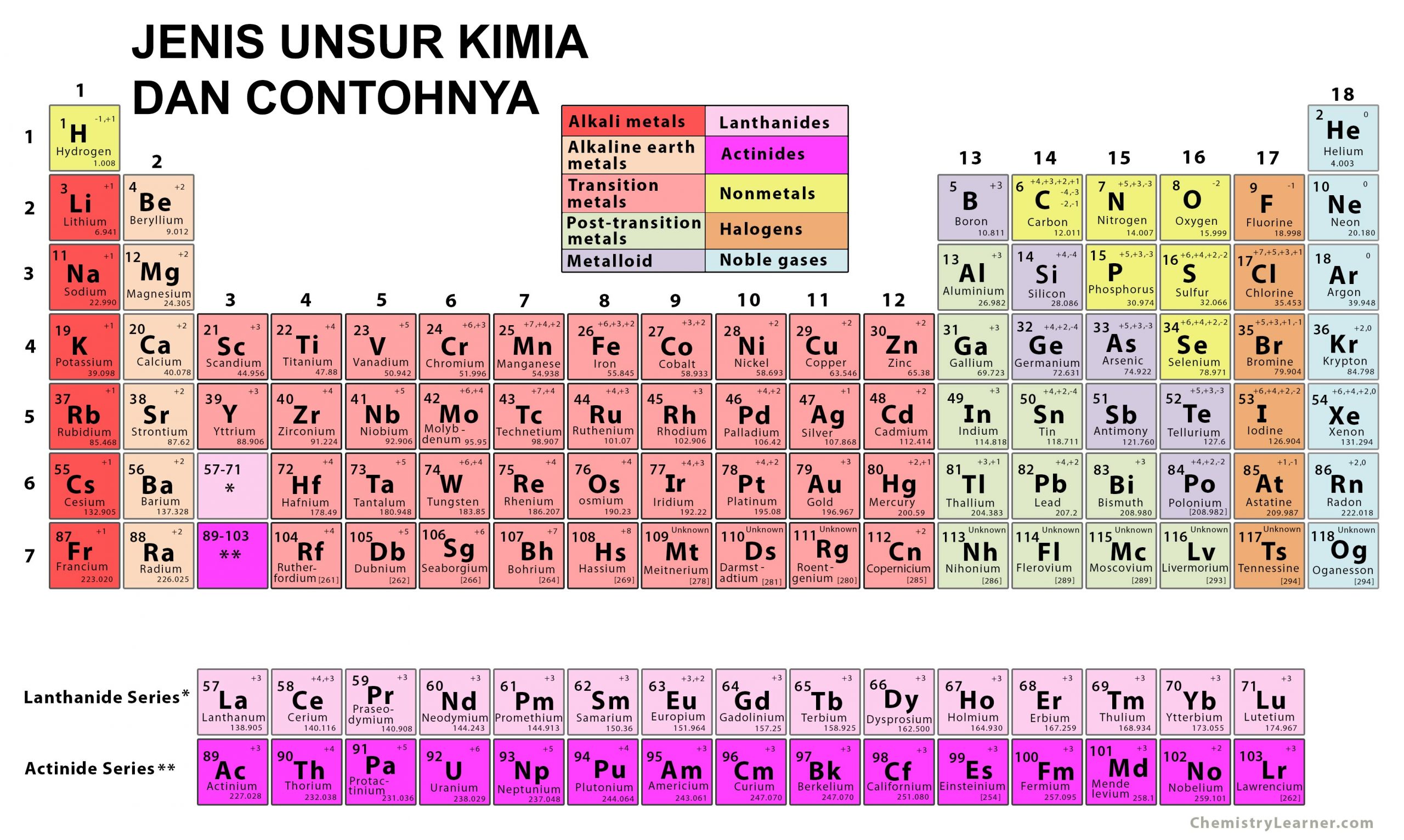
Dalam penerapan kimia unsur telah mengklasifikasikan berbagai macam unsur yang sejatinya ada dan ditemukan di dunia ini. Tabel sistem periodik adalah bagian tabel yang sangat bermanfaat di kimia unsur karena dalam tabel ini terdapat pemetaan semua jenis unsur kimia yang telah ditemukan.
Setiap unsur kimia tentunya memiliki sifat yang berbeda dan unik sehingga sangat menarik untuk dipelajari dalam kimia unsur. Bagaimana reaktivitas setiap unsur sehingga suatu unsur dapat bereaksi dengan unsur kimia yang lain untuk membentuk senyawa dapat dijelaskan dalam kimia unsur.
Unsur Kimia
Unsur kimia adalah bagian terkecil yang dapat menyusun suatu molekul dengan kata lain semua materi yang ada di dunia ini tersusun oleh gabungan unsur kimia. Tidak semua unsur kimia dapat bergabung untuk membentuk suatu molekul, melainkan hanya sebagian unsur kimia yang memiliki karakteristik tertentu saja yang mampu bereaksi dan membentuk suatu materi. Selain itu, unsur kimia juga dapat ditemukan dalam bentuk murni tanpa bergabung dengan unsur lain.
Meskipun menjadi bagian terkecil sebagai penyusun suatu materi, namun unsur kimia juga tersusun oleh beberapa bagian. Itu adalah bagian inti yakni nukleus yang dikelilingi oleh awan elektron. Nukleus memiliki muatan positif yang disebabkan karena kandungan proton yang ada di dalamnya. Elektron yang berada di sekeliling nukleus bermuatan negatif sehingga akan menetralkan muatan unsur kimia tersebut.
Elektron dalam unsur terorganisir berdasarkan orbital dan kulit elektron sesuai dengan prinsip mekanika kuantum yang membatasi keberadaan elektron dalam setiap lapisan kulit elektron. Elektron yang berada dalam kulit terluar unsur kimia ini akan berperan dalam interaksi kimia dengan unsur yang lain.
Unsur kimia dipetakan dalam tabel sistem periodik unsur yang sangat penting dalam ilmu kimia. Tabel ini merepresentasikan sangat banyak informasi penting mengenai unsur kimia dan hal tersebut akan memungkinkan para ilmuan untuk memprediksi karakteristik dan reaksi kimia yang mungkin terjadi pada setiap unsur kimia tersebut.
Model atom Rutherford mampu menjelaskan mengapa setiap jenis partikel atom ataupun unsur kimia memiliki karakteristik kimia yang berbeda dan unik. Identitas untuk setiap unsur kimia direpresentasikan dengan nomor atom (Z) yang menunjukkan jumlah proton yang terdapat dalam inti suatu atom ataupun unsur kimia.
Nomor atom ini berbeda untuk setiap unsur kimia yang terdapat dalam tabel sistem periodik. Selain itu, sifat kimia dari setiap unsur juga ditentukan oleh jumlah elektron dimana dalam atom netral, jumlah elektron sama dengan jumlah protonnya.
Unsur kimia dapat saling bereaksi ataupun bergabung untuk membentuk suatu senyawa atau molekul kimia tertentu. Sebagai contoh unsur hidrogen dapat bergabung dengan oksigen untuk membentuk molekul H2O yang kita kenal sebagai air. Namun, unsur kimia juga dapat berada dalam bentuk murni tanpa gabungan dengan unsur lain. Sebagai contoh unsur logam besi, tembaga, dan emas dapat berada dalam bentuk unsur murninya.
Jenis Unsur Kimia
Dalam tabel sistem periodik, unsur kimia telah dikelompokkan secara sempurna dan dibedakan menjadi beberapa jenis unsur kimia. Pengelompokan ini didasarkan pada sifat dan karakteristik dari masing masing unsur kimia.
-
Logam Alkali dan Alkali Tanah
Jika kita melihat tabel sistem periodik unsur bagian kiri kita akan menemukan dua grup yang merupakan logam dengan reaktivitas yang sangat tinggi. Unsur hidrogen merupakan pengecualian atau tidak termasuk ke dalam jenis logam alkali maupun alkali tanah.
Bagian kolom pertama terdiri dari logam alkali yang bersifat lunak dan berkilau. Logam bagian ini hanya memiliki satu buah elektron pada kulit elektron valensinya dimana hal ini memungkinkannya untuk dengan mudah bereaksi kimia dengan unsur lain melalui donasi elektron valensi tersebut.
Hal ini yang membuat jenis unsur ini memiliki reaktivitas yang tinggi. Dalam udara ataupun air, logam jenis ini memiliki reaktivitas yang sangat tinggi, oleh karena itu kita tidak dapat menemukan logam jenis ini dalam bentuk murninya di alam.
Sedangkan untuk logam alkali tanah memiliki elektron terluar atau valensi yaitu dua buah elektron. Hal ini membuatnya memiliki reaktivitas yang lebih rendah dibandingkan logam alkali. Namun, logam alkali tanah juga sangat jarang ditemukan dalam bentuk murni di alam.
Contoh logam alkali yaitu;
- Lithium
- Natrium
- Kalium
- Rubidium
- Cesium dan fransium.
Sedangkan contoh logam alkali tanah yaitu;
- Berilium
- Magnesium
- Kalsium
- Strontium
- Barium
- Radium
-
Logam Transisi
Logam transisi menjadi unsur kimia yang paling banyak mendominasi dalam tabel sistem periodik. Jenis unsur kimia ini terdapat pada bagian tengah tabel periodik. Logam transisi memiliki sifat berbentuk padat pada suhu ruang atau 25 oC kecuali logam merkuri dan memiliki sifat fisik yakni berwarna metalik untuk setiap logam.
Selain itu logam disini juga memiliki titik didih dan titik leleh yang tinggi serta memiliki sifat konduktivitas listrik maupun konduktivitas panas yang baik.
Logam transisi juga menjadi salah satu jenis unsur kimia yang banyak dimanfaatkan di berbagai bidang dalam kehidupan.
Contoh dari logam transisi yaitu;
- Logam Titanium
- Besi
- Nikel
- Tembaga
- Zink
- Emas
- Dan masih banyak yang lain
Tentunya kita sangat tidak asing dengan jenis jenis ikatan logam tersebut dan dapat menemukannya dalam kehidupan kita sehari hari.
-
Metaloid
Metaloid atau dapat disebut juga dengan semi logam. Jenis unsur kimia ini memiliki sifat sebagai logam dan juga sebagai non logam sehingga dikatakan sebagai semi logam. Keistimewaan sifat ini yang membuat unsur metaloid sangat bermanfaat dalam industri komponen elektronika yakni sebagai semi konduktor.
Contoh dari unsur kimia metaloid yaitu;
- Silikon
- Boron
- Germanium
- Arsenik
- Telurium
- Polonium
Seperti yang kita ketahui bahwa beberapa jenis unsur tersebut menjadi bahan utama dalam pembuatan material semi konduktor.
-
Non Logam
Jenis lain dari unsur kimia adalah unsur non logam dimana pada umumnya unsur non logam tidak memiliki warna yang berkilau. Sifat konduktivitasnya juga rendah baik konduktivitas panas maupun konduktivitas listrik atau dapat disebut sebagai isolator.
Berbeda dengan logam yang keras dan kuat, unsur non logam cenderung memiliki sifat yang lebih lemah dan mudah untuk dipatahkan. Hal itu disebabkan karena densitas yang rendah pada unsur non logam.
Unsur non logam umumnya dapat bereaksi dengan oksigen untuk menghasilkan non logam oksida. Sebagai contoh unsur sulfur bereaksi dengan oksigen menghasilkan sulfur dioksida. Contoh kimia unsur non logam yaitu hidrogen yang menjadi salah satu unsur kimia yang paling banyak di temukan di dunia ini. Kemudian ada karbon yang mampu menghasilkan banyak alotrop seperti grafit, graphene, diamond, dan lain sebagainya. Lalu ada oksigen, nitrogen, fosfor, sulfur, dan lain lain.
-
Halogen
Halogen juga dapat dikategorikan ke dalam jenis unsur kimia non logam. Unsur halogen memiliki keistimewaan yakni unsur ini memiliki tujuh elektron pada bagian kulit terluar atau elektron valensi. Sehingga unsur ini hanya membutuhkan satu elektron untuk memenuhi kulit elektronnya. Oleh karena itu unsur halogen akan mudah untuk bereaksi dengan unsur lain atau dapat dikatakan sangat reaktif.
Unsur golongan halogen ini dapat dengan mudah bereaksi dengan unsur logam untuk membentuk suatu senyawa seperti unsur logam natrium bereaksi dengan klorin menghasilkan natrium klorida (NaCl) yang kita kenal sebagai garam dapur. Contoh lain dari unsur kimia halogen selain klor yaitu flor, brom, yodium, astatin, dan tenesin.
Jenis unsur kimia terakhir yaitu unsur gas mulia yang dapat kita temukan pada bagian paling kanan dari tabel sistem periodik. Kelompok gas mulia terdiri dari unsur yang berwujud gas. Unsur gas mulia memiliki elektron valensi yang sudah penuh atau berjumlah 8 elektron.
Hal ini membuatnya bersifat sangat stabil atau tidak reaktif karena cenderung mempertahankan elektron dan tidak menarik elektron dari unsur lain. Fakta yang mendukung ini yaitu bahwa gas mulia dapat ditemukan dengan mudah dalam bentuk murninya di alam. Gas mulia bersifat inert atau tidak bereaksi dengan unsur lain, tidak berwarna, dan tidak berasa.
Contoh gas mulia yaitu
- Helium
- Neon
- Argon
- Kripton
- Xenon
- Radon
Demikian pembahasan lengkap yang bisa kami tuliskan pada semua pembaca berkaitan dengan materi jenis unsur kimia dan contohnya. Semoga artikel ini dapat menambah wawasan dan bermanfaat terutama bagi kalian yang sedang membutuhkannya.


