Konsep dasar ilmu kimia secara umum adalah studi tentang materi dan energi yang mencakup semua bahasan terkait dengan kematerian yang ada di alam semesta. Dimana bahasan ini secara lengkap berada dalam penerapan kimia dasar yang biasanya dipelajari berbagai klasifikasi unsur kimia, senyawa, dan bahan material yang didasarkan pada komposisinya.
Oleh karena itulah ilmu kimia tak pernah lepas dari kehidupan manusia, karena hal ini lah mengapa ilmu kimia penting untuk dipelajari. Dalam mempelajari ilmu kimia, tahap pertama yang harus dipelajari adalah bagian kimia dasar.
Kimia Dasar
Apa yang dipelajari dalam ilmu kimia pada hakekatnya ialah semua prosedur yang dilakukan sistematis dan dapat direproduksi yang berartinya dapat dilakukan ulang oleh orang yang berbeda dan dalam waktu yang berbeda serta metode hipotesisnya juga diuji secara ilmiah.
Oleh karena itulah keberadaan ilmu kimia erat kaitannya dengan fisika dan ilmu biologi karena memang ketiga ilmu tersebut saling berkaitan.
Pengertian Kimia Dasar
Kimia dasar adalah bagian integralistik dari ilmu kimia yang senantisa mempelajari hal-hal yang mendasar dan prinsip dalam kimia, sebagimana memahami konsep materi, mempelajari sifat-sifatnya, bagaimana dan mengapa zat tersebut dapat bergabung ataupun terpisah untuk membentuk zat lain dan bagaimana zat tersebut saling berinteraksi.
Disisi lainnya, sebelum seorang ahli kimia dapat bekerja di lab dengan berbagai alat laboratorium kimia untuk melakukan eksperimen atau penelitian, maka kimia dasar adalah hal pertama yang harus di kuasai.
Pengertian Kimia Dasar Menurut Para Ahli
Adapun definisi kimia dasar menurut para ahli, antara lain;
- Raymond Chang, Kimia dasar adalah cabang kimia yang mencakup konsep-konsep fundamental, prinsip-prinsip dasar, dan teori-teori yang menjadi dasar bagi semua cabang ilmu kimia lainnya.
- Zumdahl dan Zumdahl, Arti kimia dasar adalah studi tentang sifat-sifat materi, perubahan yang dialami oleh materi, dan energi yang terlibat dalam perubahan tersebut.
- IUPAC (International Union of Pure and Applied Chemistry), Kimia dasar adalah cabang ilmu kimia yang mempelajari dasar-dasar konsep kimia seperti atom, molekul, struktur zat, reaksi kimia, dan sifat-sifat materi.
Jenis Hukum Dasar Kimia

Setidaknya terdapat beberapa hukum-hukum kimia dasar yang harus diketahui. Adapun untuk beberapa bunyi hukum dasar kimia. Antara lain;
-
Hukum Kekekalan Massa
“Tidak ada sesuatu yang datang dari ketiadaan” bunyi ini merupakan ide dalam filsafat Yunani kuno yang berpendapat bahwa apa yang ada saat ini akan selalu ada, karena tidak ada materi baru yang dapat muncul jika sebelumnya tidak ada. Antoine Lavoiser seorang ilmuwan menyatakan kembali prinsip kimia ini dengan hukum kekekalan masa. “Atom tidak dapat dibuat atau dihancurkan, tetapi dapat dipindahkan dan diubah menjadi partikel yang berbeda”.
Hukum ini mengatakan bahwa ketika terjadi definisi reaksi kimia menata ulang atom menjadi produk baru, maka massa reaktan (bahan awal reaksi) akan sama dengan massa produk (hasil reaksi). Hukum kekekalan massa ini menyatakan bahwa massa total yang ada sebelum terjadinya reaksi sama dengan massa totoal setelah reaksi. Hukum kekekalan massa ini ditemukan oleh Lavoiser dari hasil eksperimen yang dilakukannya.
Lavoiser membakar ikatan logam merkuri dengan berat tertentu dalam suatu wadah tertutup dan menimbang beratnya. Volume udara yang berada di dalam wadah tertutup tersebut setelah pembakaran ternyata berkurang, sedangkan merkuri telah berubah menjadi oksida merkuri dengan massa yang lebih tinggi daripada massa sebelumnya.
Hasilnya didapatkan bahwa ternyata penambahan massa merkuri tersebut sama dengan massa volume udara atau oksigen yang hilang sehingga hasil total penimbangan sebelum dan sesudah reaksi juga sama.
Merkuri + Oksigen → Merkuri Oksida
Berdasarkan eksperimennya, Lavoiser membuat suatu keismpulan dengan nama hukum kekekalan massa dengan bunyi “Massa zat sebelum dan sesudah reaksi tetap”.
-
Hukum Perbandingan Tetap
Joseph Proust merupakan orang yang merumuskan hukum perbandingan tetap atau biasa dikenal dengan hukum proust. Hukum ini menyatakan bahwa jika suatu senyawa dapat dipecah menjadi unsur-unsur penyusunnya, maka massa konstituen akan selalu memiliki proporsi yang sama terlepas dari jumlah atau sumber zat aslinya.
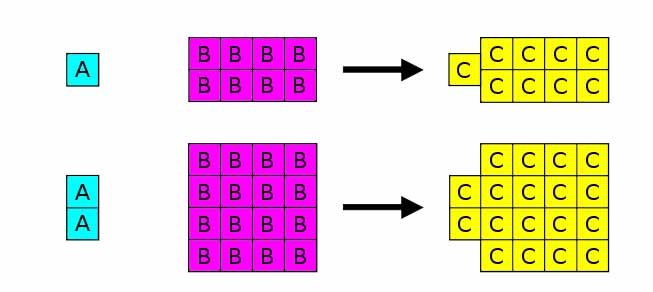
Secara mudahnya dapat di ilustrasikan pada gambar contoh reaksi diatas. Jika 1 gram A dapat bereaksi dengan 8 gram B, maka dengan mengikuti hukum proust ini 2 gram A harus bereaksi dengan 16 gram B. Jika 1 gram A bereaksi dengan 8 gram B, maka akan dihasilkan 9 gram C dan jika 2 gram A bereaksi dengan 16 gram B, akan dihasilkan 18 gram C.
Hukum perbandingan tetap menyatakan bahwa dalam suatu jenis zat kimia tertentu, unsur-unsurnya selalu digabungkan dalam proporsi yang sama. Hukum ini berlaku ketika suatu zat saling bereaksi untuk membentuk produk yang sama.
-
Hukum Perbandingan Berganda
Selain dua unsur bereaksi membentuk satu produk, banyak kombinasi zat juga dapat bereaksi membentuk lebih dari satu produk.
Dalam kasus ini, hukum perbandingan bergana (Hukum Dalton) menyatakan bahwa berat satu elemen yang bergabung dengan elemen lainnya adalah kelipatan bilangan bulat satu sama lainnya. Hal ini dapat digambarkan pada reaksi nitrogen yang membentuk sifat nitrogen oksida dalam beberapa bentuk yang dapat dilihat pada gambar berikut:
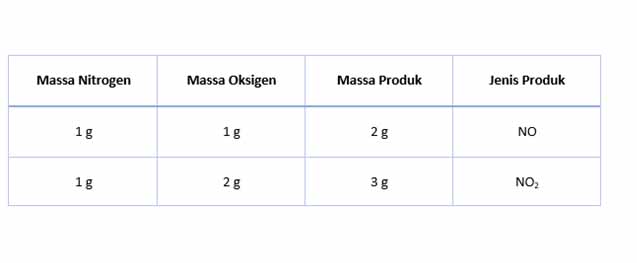
Hukum perbandingan berganda diaplikasikan pada senyawa nitrogen oksida (NOX). Dengan menggunakan massa oksigen yang sama untuk membentuk nitrogen oksida dengan nitrogen dengan massa yang berbeda, maka akan dihasilkan senyawa yang berbeda dengan massa yang sesuai dengan kelipatan bilangan bulatnya.
Hukum perbandingan berganda berbunyi “Jika dua elemen dapat membentuk lebih dari satu senyawa, maka massa satu elemen dikombinasikan dengan massa tetap dari elemen kedua dengan membentuk rasio bilangan bulat untuk menentukan massa produknya”.
-
Hukum Perbandingan Volume
Hukum perbandingan volume dirumuskan oleh Gay-Lussac dimana ketika suatu gas bereaksi bersama, maka mereka akan melakukannya dalam volume yang menghasilkan rasio bilangan bulat sederhana dimana reaksi dilakukan dibawah kondisi suhu dan tekanan yang sama.
Adapun untuk hukum ini dapat dilihat dalam contoh kasus reaksi berikut;
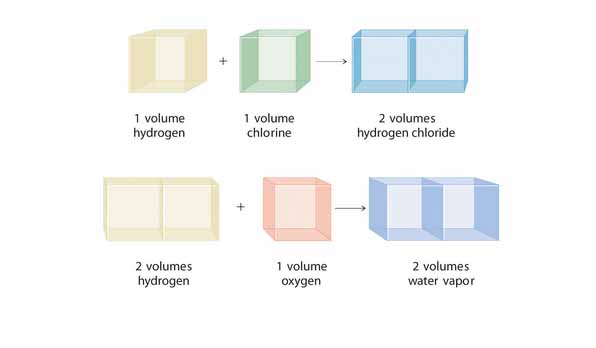
Ketika 1 satuan volume dari gas hidrogen bereaksi dengan 1 satuan volume dari gas klorin, maka membentuk 2 volume dari gas hidrogen klorida dengan rasion volumenya adalah 1:1:2. Sedangkan pada reaksi 2 volume hidrogen dengan 1 volume oksigen menghasilkan gas 2 volume H2O dengan rasio 2:1:2. Rasio ini dipengaruhi oleh rumus dari senyawa atau produk yang dihasilkan.
Hukum Gay-Lussac menyatakan bahwa “Dalam kondisi tekanan dan suhu yang sama, maka volume gas yang bereaksi serta volume gas produk dari reaksi merupakan perbandingan bilangan bulat sederhana”.
Macam Cabang Ilmu Kimia
Terdapat beberapa cabang ilmu kimia setelah kimia dasar yang dapat dipelajari. Yaitu;
-
Kimia Organik
Kimia organik adalah cabang ilmu kimia yang mempelajari senyawa yang mengandung unsur karbon dan hidrogen atau berada dalam makhluk hidup. Ahli kimia organik dapat memahami struktur, sifat, dan jenis reaksi dalam senyawa tersebut serta dapat mengidentifikasi dan mengklasifikasikannya.
Adapun untuk contoh kimia organik banyak diterapkan dalam industri farmasi, karet, bahan bakar, plastik, kosmetik, zat warna, detergen, pertanian, dan lain sebagainya.
-
Kimia Anorganik
Kimia anorganik adalah reaksi dan semua sifat senyawa kimia yang tidak memiliki ikatan kimia karbon dan hidrogen. Dengan kata lain, kimia anoranik mempelajari senyawa yang bukan berasal dari materi hidup. Untuk contoh kimia organik juga banyak diterapkan dalam industri katalis, material, pigmen, pelapis, dan medis.
-
Kimia Fisik
Cabang ilmu kimia fisika mempelajari sifat fisik dari senyawa kimia menggunakan hukum dan konsep fisika seperti gerak, energi, gaya, waktu, termodinamika, kuantum, mekanika dan dinamika. Dengan formula kimia fisika, ahli kimia dapat mengukur sifat fisik zat kimia dan menentukan efek dari fenomena tertentu pada zat kimia.
-
Kimia Analitik
Cabang ilmu kimia ini berkaitan dengan proses pemisahan, identifikasi, dan kuantifikasi zat kimia secara analitik dengan suatu sampel tertentu.
Ilmu ini memungkinkan ahli kimia untuk menentukan zat-zat kimia yang berada dalam bahan tertentu. Kimia analisis memiliki cakupan yang sangat luas dalam aplikasinya. Untuk contoh kimia analitik ini seperti dalam lingkungan forensik, analisa klinis, analisa bahan, dan bioanalisis.
-
Biokimia
Biokimia adalah cabang ilmu kimia yang mempelajari struktur, komposisi, dan reaksi kimia dalam sistem kehidupan. Biokimia menggabungkan biologi dengan kimia untuk kasus perubahan mendasar yang terjadi dalam sistem makhluk hidup. Adapun untuk contoh penerapan biokimia sangat luas seperti dalam kedokteran, ilmu pangan, dan pertanian.
Dari penjelasan yang dikemukakan, dapatlah dikatakan bahwa materi kimia dasar sejatinya berhubungan dengan disiplin pengetahuan yang terjad secara sistematis dengan memahami komposisi, sifat dan aktivitas zat-zat baik itu organik maupun anorganik serta berbagai bentuk unsur materi.
Oleh karena itulah kimia juga sering didefinisikan sebagai studi tentang materi dan reaksi yang terjadi dalam materi tersebut. Ahli kimia dapat membuat senyawa baru dan memahami bagaimana suatu reaksi dapat menghasilkan senyawa tersebut.
Adapun disisi lainnya terdapat beberapa bentuk hukum kimia dasar dengan prinsip untuk menganalisa serta mengidentifikasi suatu peristiwa yang terjadi secara kimiawi.
Nah, itulah tadi pengulasan secara lengkapnya mengenai pengertian kimia dasar, hukum, dan cabangnya. Semoga melalui saja tulisan ini bisa memberikan wawasan serta menambah referensi mendalam bagi segenap pembaca sekalian.